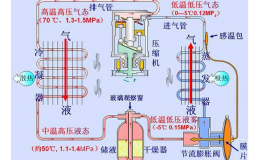
在自然界,一切物质都是由原子构成的。而物质内部的原子,则可能是紊乱地堆置(如玻璃、塑料等)或呈一定规律排列(如金属材料)。所有的固体金属,其原子均按一定的规律排列,被称为晶体。为了便于描述和分析品体中原子排列的规律,可以用假想的线条将各原子中心连接起来,使之构成一空问格子,每个原子中心均位于空间格子的各个结点上。这种用以描绘原子在晶体中排列方式的空间格子称为“结晶格子”,简称“晶格”[图3-1(a)],用晶格来描述晶体结构还很不方便,为了简便起见,通常从晶格中选取一个能反映晶格特征的最小几何单元来描述各种晶体结构,这个最小几何单元称为“晶胞”,即晶格是由晶胞在空间重复排列而成。
金属的晶格形式最常见的有两种,即体心立方晶格和面心立方晶格。图3-1(b)和图3一1(c)分别表示这两种晶格的晶胞。
(1)体心立方晶胞。它是一个立方体,在立方体的顶角上各有一个原子,而在立方体的中心又有一个原子[图3一1(b)]。具有体心立方晶格的金属有910℃以下的铁(称为a-Fe),室温下的铬、钨、钼、钒、铌等。
(2)面心立方晶胞。它也是一个立方体,在立方体的八个顶角上也各有一个原子,此外,在立方体的六个面的中心也各有一个原子[图3-1(c)],具有面心立方晶格的金属有910~1 390℃的铁(称为ϒ-Fe),铜、铝、金、银、镍、铅等。
由于晶体结构的不同,晶体在晶体性能上也必然表现出某些不同的特性。一般来讲,具有面心立方晶格的金属均具有良好的塑性和韧性,特别是没有冷脆性(冷脆性是指在低温下金属的塑性和韧性随温度降低而急剧降低的性能)。因此,像铜、铝、金、银等面心立方结构的金属可轧成很薄的金属箔,拉成很细的金属丝,像铜、铝、镍等也是良好的低温材料;具有体心立方品格的金属均具有较高的硬度、强度和熔点,但是塑性和韧性较低,且具有冷脆性,因此,像α-Fe,铬、钨、钼等体心立方结构的金属均可作为高强度、高温合金的基础。